Сравнение мультипараметрического и бипараметрического протоколов магнитно-резонансной томографии для выявления рака предстательной железы рентгенологами с различным опытом
- Авторы: Васильев Ю.А.1, Омелянская О.В.1, Владзимирский А.В.1, Гележе П.Б.1,2, Решетников Р.В.1, Гончар А.П.1, Блохин И.А.1, Абдуллин И.И.1, Киева И.Н.3
-
Учреждения:
- Научно-практический клинический центр диагностики и телемедицинских технологий
- Акционерное общество «Европейский Медицинский Центр»
- Детская городская клиническая больница № 9 имени Г.Н. Сперанского
- Выпуск: Том 4, № 4 (2023)
- Страницы: 455-466
- Раздел: Оригинальные исследования
- Статья получена: 15.04.2023
- Статья одобрена: 15.06.2023
- Статья опубликована: 15.12.2023
- URL: https://jdigitaldiagnostics.com/DD/article/view/322816
- DOI: https://doi.org/10.17816/DD322816
- ID: 322816
Цитировать
Аннотация
Обоснование. Проведение магнитно-резонансной томографии позволяет выявить клинически значимый рак предстательной железы, диагностировать экстракапсулярную экстензию, стадировать онкологический процесс. Протокол сканирования, включающий только Т2-взвешенные и диффузионно-взвешенные изображения, представляет собой жизнеспособную альтернативу мультипараметрической магнитно-резонансной томографии при условии сохранения высокой диагностической точности теста. В недавних исследованиях диагностическая точность бипараметрической и мультипараметрической магнитно-резонансной томографии в выявлении рака предстательной железы продемонстрировала незначительные различия.
Цель ― сравнение диагностической точности бипараметрической и мультипараметрической магнитно-резонансной томографии для выявления клинически значимого рака предстательной железы по системе PI-RADS v2.1 с использованием мультифокальной биопсии под контролем магнитно-резонансной томографии в качестве золотого стандарта.
Материалы и методы. Данное исследование является ретроспективным. Мы изначально обработали записи историй болезни 126 пациентов. Критериями включения в исследование были наличие мультипараметрической магнитно-резонансной томографии по стандарту PI-RADS 2.1, клинической информации об уровнях свободного и связанного простатспецифического антигена крови, мультифокальной биопсии предстательной железы при соблюдении временного интервала между магнитно-резонансной томографией и биопсией не более 14 дней. Три исследователя (врачи-рентгенологи с опытом работы менее 2 лет, от 2 до 5 лет, более 5 лет соответственно) независимо друг от друга оценивали бипараметрическую магнитно-резонансную томографию предстательной железы на предмет наличия патологических очагов. Спустя 2 недели исследователи оценивали датасет мультипараметрической магнитно-резонансной томографии предстательной железы. Каждый выявленный очаг, начиная с категории PI-RADS 3, сопоставлялся с результатом мультифокальной фьюжн-биопсии. Результат биопсии представлялся в виде суммы значений по шкале Gleason, при этом к клинически значимым данным биопсии относилась сумма Gleason 7 и выше. Опухолевыми очагами по данным магнитно-резонансной томографии считались находки, соответствующие критериям PI-RADS 4 и 5.
Результаты. Наилучшие показатели чувствительности и специфичности выявления очагов на магнитно-резонансной томографии предстательной железы ― 62,5 и 74,6% соответственно. Наивысшая достигнутая диагностическая точность составила 70,1%. Мультипараметрическая магнитно-резонансная томография обладает более высокими показателями специфичности выявления очагов предстательной железы при интерпретации рентгенологами с опытом работы менее 2 лет и более 5 лет.
Заключение. Как бипараметрическая, так и мультипараметрическая магнитно-резонансная томография предстательной железы продемонстрировала неоптимальные показатели диагностической точности. Имеется тенденция к улучшению чувствительности и специфичности метода с увеличением опыта работы рентгенолога. Бипараметрические протоколы сканирования предстательной железы имеют безусловное экономическое преимущество перед мультипараметрическими за счёт отсутствия расходов на контрастное вещество и расходные материалы и значительного снижения времени загрузки МР-сканера, однако их использование может привести к снижению диагностической точности метода.
Ключевые слова
Полный текст
Список сокращений
ДВИ ― диффузионно-взвешенные изображения
ДКУ ― динамическое контрастное усиление
МРТ ― магнитно-резонансная томография
бпМРТ ― бипараметрическая магнитно-резонансная томография
мпМРТ ― мультипараметрическая магнитно-резонансная томография
Т2-ВИ ― Т2-взвешенные изображения
ТрУЗИ ― трансректальное ультразвуковое исследование
SS-EPI (single short echo planar pulse) ― одиночный короткий эхо-планарный импульс
TSE (turbo-spin-echo) ― турбо-спиновое эхо
ОБОСНОВАНИЕ
При клиническом ведении пациентов с повышенным уровнем простатспецифического антигена важную роль играет мультипараметрическая магнитно-резонансная томография (мпМРТ), включающая Т2-взвешенные изображения (Т2-ВИ), диффузионно-взвешенные изображения (ДВИ) и динамическое контрастное усиление (ДКУ).
Проведение МРТ позволяет выявить клинически значимый рак предстательной железы, диагностировать экстракапсулярную экстензию, стадировать онкологический процесс. Для стандартизации сбора данных МРТ, интерпретации изображений Американским колледжем радиологии (American College of Radiology, ACR), Европейским урологическим обществом (European Symposium on Urogenital Radiology, ESUR) в 2019 году была выпущена система оценки данных и формирования заключения (Prostate Imaging Reporting and Data System, PI-RADS) в виде версии 2.1 (v2.1) [1].
С 2020 года европейские и американские руководства по урологии рекомендуют проводить мультипараметрическую МР-визуализацию (мпМРТ) у не подвергавшихся биопсии мужчин с подозрением на рак предстательной железы [2, 3]. Согласно данным клинического исследования O. Rouvière и соавт. [3], выполнение мпМРТ при повышении концентрации простатспецифического антигена позволяет избежать ненужной биопсии у 27% мужчин. Поскольку большинство мужчин подвергаются исследованию уровня простатспецифического антигена в течение всей жизни, применение этих рекомендаций приводит к значительному увеличению спроса на МРТ предстательной железы.
ДКУ играет относительно небольшую роль в определении категории оценки по PI-RADS, поскольку используется только для дифференциальной диагностики очагов категорий 3 и 4 по PI-RADS, локализованных в периферической зоне. Кроме того, применение ДКУ создаёт риск развития системного нефрогенного фиброза у пациентов, страдающих почечной недостаточностью. В связи с этим растёт интерес к проведению сокращённых протоколов МРТ простаты без использования ДКУ, или бипараметрической МРТ (бпМРТ) [4–6].
Протокол сканирования, включающий только Т2-ВИ и ДВИ, представляет собой жизнеспособную альтернативу мпМРТ при условии сохранения высокой диагностической точности теста [7]. В недавних исследованиях диагностическая точность бпМРТ и мпМРТ в выявлении рака предстательной железы продемонстрировала незначительные различия [6]. Успешные попытки создать протокол бпМРТ показали сопоставимые с мпМРТ показатели неоднородности яркости, разрешающей способности и нелинейности [8].
В ответ на растущий интерес к проведению бпМРТ руководящий комитет PI-RADS выпустил консенсусное заявление, в котором призвал «получить более качественные данные, прежде чем давать научно обоснованные рекомендации относительно бпМРТ в качестве начального диагностического теста» [9].
Цель исследования ― сравнение диагностической точности бпМРТ и мпМРТ для выявления клинически значимого рака предстательной железы по системе PI-RADS v2.1 с использованием таргетной фьюжн-биопсии в качестве золотого стандарта.
Задачи исследования ― выявление чувствительности и специфичности мпМРТ и бпМРТ в отношении диагностики клинически значимого (PI-RADS 4 и выше) рака предстательной железы; сравнение чувствительности и специфичности мпМРТ и бпМРТ при анализе рентгенологами с разным опытом; оценка согласованности врачей с разным опытом в анализе мпМРТ и бпМРТ.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования
Данное исследование является обсервационным одноцентровым ретроспективным выборочным.
Критерии соответствия
Критерии включения: наличие мпМРТ по стандарту PI-RADS 2.1; клиническая информация об уровнях свободного и связанного простатспецифического антигена крови; проведённая таргетная МРТ/ТрУЗИ фьюжн-биопсия при соблюдении временного интервала между МРТ и биопсией не более 14 дней.
Критерии невключения: технические артефакты или несоответствие МРТ предстательной железы стандарту PI-RADS 2.1; отсутствие одного или нескольких клинических маркёров; увеличенный временной интервал между проведением мпМРТ и биопсией.
Критерии исключения: выраженные артефакты мпМРТ, не позволяющие адекватно оценить исследование, а также неинформативные результаты биопсии.
Согласно приведённым критериям, рентгенологи с опытом менее 2 лет и более 5 лет исключили из выборки 19 пациентов, рентгенолог с опытом от 2 до 5 лет ― 23 пациента.
Условия проведения
Набор пациентов, которым выполнялась МРТ предстательной железы и мультифокальная фьюжн-биопсия, осуществлялся на базе частного медицинского учреждения АО «Европейский Медицинский Центр».
Продолжительность исследования
Для проведения исследования отобраны записи электронных историй болезни за период с 01.01.2022 по 01.06.2022.
Описание медицинского вмешательства
Обработаны записи историй болезни 126 пациентов. мпМРТ предстательной железы выполнялась на томографе Siemens Aera 1,5 T 4G (Германия) с использованием катушки для тела. Протокол сканирования включал в себя следующий набор импульсных последовательностей (табл. 1). После выгрузки и анонимизации из мпМРТ элиминировались серии изображений с ДКУ, после чего формировался датасет исследований бпМРТ. Три исследователя (врачи-рентгенологи с опытом работы менее 2 лет, от 2 до 5 лет, более 5 лет) независимо друг от друга оценивали бпМРТ предстательной железы на предмет наличия патологических очагов. Выявленному очагу присваивалась категория от 1 до 5 (по данным ДВИ ― для очагов периферической зоны, по данным Т2-ВИ ― для очагов переходной зоны в соответствии с PI-RADS v2.1), определялась общая категория PI-RADS для всей железы. Референсный метод ― гистопатологическое исследование предстательной железы на основе таргетной МРТ/ТрУЗИ фьюжн-биопсии.
Таблица 1. Протокол мультипараметрической магнитно-резонансной томографии предстательной железы
Импульсная последовательность | Ориентация срезов | TE/TR, мсек | FOV, мм | Размер пикселя, мм | Толщина среза / перекрытие, мм | Ориентировочное время сканирования, мин |
Т2-ВИ TSE | Сагиттальная | 120/3800 | 250×250 | 1×1 | 3/0,3 | 2:26 |
Т2-ВИ TSE | Аксиальная | 110/3938 | 180×180 | 0,45×0,6 | 2,5/0 | 3:33 |
ДВИ SS-EPI | Аксиальная | 87/2425 | 160×160 | 1,25×1,32 | 3/0,3 | 6:50 |
Т2-ВИ TSE | Корональная | 110/2500 | 160×160 | 0,38×0,42 | 2,5/0 | 4:50 |
Т1-ВИ с ДКУ, временное разрешение 15 сек | Аксиальная | 2,3/4,6 | 250×250 | 0,9×1 | 3/0 | 5:46 |
Т1-ВИ после КУ | Аксиальная | 1,3/2,3 | 400×350 | 1,6×1,7 | 4/0 | 0:21 |
Примечание. ДВИ ― диффузионно-взвешенные изображения; ДКУ ― динамическое контрастное усиление; КУ ― контрастное усиление; Т2-ВИ ― Т2-взвешенные изображения; SS-EPI ― одиночный короткий эхо-планарный импульс;TSE (turbo-spin-echo) ― турбо-спиновое эхо.
Спустя 2 недели исследователи оценивали датасет мпМРТ предстательной железы, включающий в числе прочих серии с динамическим контрастным усилением. Исследователи не имели доступа к результатам биопсии во время интерпретации МРТ. Согласно PI-RADS 2.1 [1], информация о раннем контрастном усилении позволяет достоверно дифференцировать очаги категорий PI-RADS 3 и 4, локализованные в периферической зоне.
Основной исход исследования
Соответствие выявленного очага предстательной железы по данным биМРТ или мпМРТ результатам гистопатологического исследования.
Методы регистрации исходов
Информация о выявленных очагах вносилась в таблицу с указанием локализации с учётом сегментации по PI-RADS 2.1. Центральная зона и фибромускулярная строма не включались в оценку.
Каждый выявленный очаг, начиная с категории PI-RADS 3, сопоставлялся с результатом таргетной МРТ/ТрУЗИ фьюжн-биопсии. При фьюжн-биопсии врач получает изображение предстательной железы с помощью ультразвука; при этом осуществляется наложение ультразвука на заранее сохраненную МРТ предстательной железы (как правило, Т2-ВИ в аксиальной плоскости). В результате слияния создаётся трёхмерная реконструкция простаты, и на реконструированной модели происходит прицеливание и отслеживание мест биопсии.
Результат биопсии представлялся в виде суммы значений по шкале Gleason [10], при этом к клинически значимым данным биопсии относилась сумма Gleason 7 и выше. Опухолевыми очагами по данным МРТ считались находки, соответствующие критериям PI-RADS 4 и 5.
Этическая экспертиза
На проведение исследования получено согласие локального этического комитета АО «Европейский Медицинский Центр» (протокол заседания № 1 от 24.04.2023).
Статистический анализ
Отдельно для каждого обработанного экспертами датасета рассчитывались показатели диагностической эффективности, включая индекс Юдена (Youden). Согласованность результатов между экспертами оценивалась в виде процентов и каппы Флейсса (Fleiss’s kappa).
Расчёты проводились с помощью среды R 4.1.31 с использованием пакетов irr2 и dplyr3.
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
Общее число проанализированных наборов данных пациентов для рентгенологов с опытом менее 2 лет и более 5 лет составило 107, для рентгенолога с опытом работы от 2 до 5 лет ― 103.
Основные результаты исследования
Наилучшими показателями чувствительности и специ-фичности бпМРТ для выявления патологических очагов предстательной железы были 70,0 и 67,2% соответственно. Наилучшие значения чувствительности и специфичности мпМРТ для выявления патологических очагов предстательной железы составили 62,5 и 74,6% соответственно.
Нежелательных явлений не отмечено.
Количество выявленных опухолевых очагов предстательной железы рентгенологами с различным опытом работы представлено в табл. 2. Данные по диагностической точности экспертов в оценке бпМРТ приведены в табл. 3, в оценке мпМРТ ― в табл. 4. Согласованность результатов между экспертами представлена в табл. 5 (в долях единицы) и 6 (каппа Флейсса).
Таблица 2. Абсолютное и относительное количество очагов предстательной железы, выявленное рентгенологами с различным опытом работы, n (%)
Опыт работы, лет | Протокол | Истинно положительный | Истинно отрицательный | Ложноположительный | Ложноотрицательный |
<2 | бпМРТ | 19 (17,8) | 47 (43,9) | 20 (18,7) | 21 (19,6) |
мпМРТ | 19 (17,8) | 52 (48,6) | 15 (14,0) | 21 (19,6) | |
От 2 до 5 | бпМРТ | 31 (29,8) | 23 (22,1) | 42 (40,4) | 8 (7,7) |
мпМРТ | 32 (30,8) | 19 (18,3) | 46 (44,2) | 7 (6,7) | |
>5 | бпМРТ | 28 (26,2) | 45 (42,1) | 22 (20,6) | 12 (11,2) |
мпМРТ | 25 (23,4) | 50 (46,7) | 17 (15,9) | 15 (14,0) |
Примечание. БпМРТ/мпМРТ ― бипараметрическая/мультипараметрическая магнитно-резонансная томография.
Таблица 3. Сравнение диагностических критериев выявления патологических очагов предстательной железы по PI-RADS 2.1 при помощи бипараметрической магнитно-резонансной томографии рентгенологами с различным опытом
Опыт работы, лет | Чувствительность | Специфичность | Точность | Прогностическое значение | Индекс Юдена | |
Положительное | Негативное | |||||
<2 | 47,5 (31,5–63,9) | 70,2 (57,7–80,7) | 61,7 (51,8–70,9) | 48,7 (36,8–60,8) | 69,1 (61,6–75,8) | 0,177 |
От 2 до 5 | 79,5 (63,5–90,7) | 35,4 (23,9–48,2) | 51,9 (41,9–61,8) | 42,5 (36,7–48,4) | 74,2 (58,8–85,3) | 0,149 |
>5 | 70,0 (53,5–83,4) | 67,2 (54,6–78,2) | 68,2 (58,5–76,9) | 56,0 (46,1–65,5) | 79,0 (69,4–86,1) | 0,372 |
Примечание. Данные представлены в виде медианы и 95% доверительного интервала.
Таблица 4. Сравнение диагностических критериев выявления патологических очагов предстательной железы по PI-RADS 2.1 при помощи мультипараметрической магнитно-резонансной томографии рентгенологами с различным опытом
Опыт работы, лет | Чувствительность | Специфичность | Точность | Прогностическое значение | Индекс Юдена | |
Положительное | Негативное | |||||
<2 | 47,5 (31,5–63,9) | 77,6 (65,8–86,9) | 66,4 (56,6–75,2) | 37,4 (28,2–47,3) | 55,9 (42,2–68,8) | 0,251 |
От 2 до 5 | 82,1 (66,5–92,5) | 28,2 (18,6–41,8) | 49,0 (39,1–59,0) | 41,0 (35,9–46,3) | 73,1 (55,7–85,4) | 0,113 |
>5 | 62,5 (45,8–77,3) | 74,6 (62,5–84,5) | 70,1 (60,5–78,6) | 59,5 (47,8–70,3) | 76,9 (68,6–83,6) | 0,371 |
Примечание. Данные представлены в виде медианы и 95% доверительного интервала.
Таблица 5. Согласованность результатов между экспертами (в долях единицы)
Протокол Опыт работы | бпМРТ, <2 лет | мпМРТ, <2 лет | бпМРТ, >5 лет | мпМРТ, >5 лет | бпМРТ, 2–5 лет | мпМРТ, 2–5 лет |
бпМРТ, <2 лет | 1 | 0,798 | 0,558 | 0,673 | 0,413 | 0,356 |
мпМРТ, <2 лет | 1 | 0,654 | 0,817 | 0,356 | 0,298 | |
бпМРТ, >5 лет | 1 | 0,808 | 0,442 | 0,452 | ||
мпМРТ, >5 лет | 1 | 0,413 | 0,357 | |||
бпМРТ, 2–5 лет | 1 | 0,904 | ||||
мпМРТ, 2–5 лет | 1 |
Примечание. бпМРТ/мпМРТ ― бипараметрическая/мультипараметрическая магнитно-резонансная томография.
Таблица 6. Согласованность результатов между экспертами (каппа Флейсса)
Протокол Опыт работы | бпМРТ, <2 лет | мпМРТ, <2 лет | бпМРТ, >5 лет | мпМРТ, >5 лет | бпМРТ, 2–5 лет | мпМРТ, 2–5 лет |
бпМРТ, <2 лет | 1 | 0,669 | 0,318 | 0,482 | 0,195 | 0,136 |
мпМРТ, <2 лет | 1 | 0,446 | 0,693 | 0,129 | 0,087 | |
бпМРТ, >5 лет | 1 | 0,699 | 0,206 | 0,229 | ||
мпМРТ, >5 лет | 1 | 0,194 | 0,165 | |||
бпМРТ, 2–5 лет | 1 | 0,846 | ||||
мпМРТ, 2–5 лет | 1 |
Примечание. бпМРТ/мпМРТ ― бипараметрическая/мультипараметрическая магнитно-резонансная томография.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
К первоочередному выводу нашей работы можно отнести невысокие показатели диагностической эффективности МРТ предстательной железы. Так, значения чувствительности и специфичности выявления очагов не превышали 62,5 и 74,6% соответственно с максимальной диагностической точностью 70,1%. Полученные показатели не позволяют рассматривать МРТ как метод ранней диагностики, исходя, в первую очередь, из неоптимально низких значений чувствительности (рис. 1).
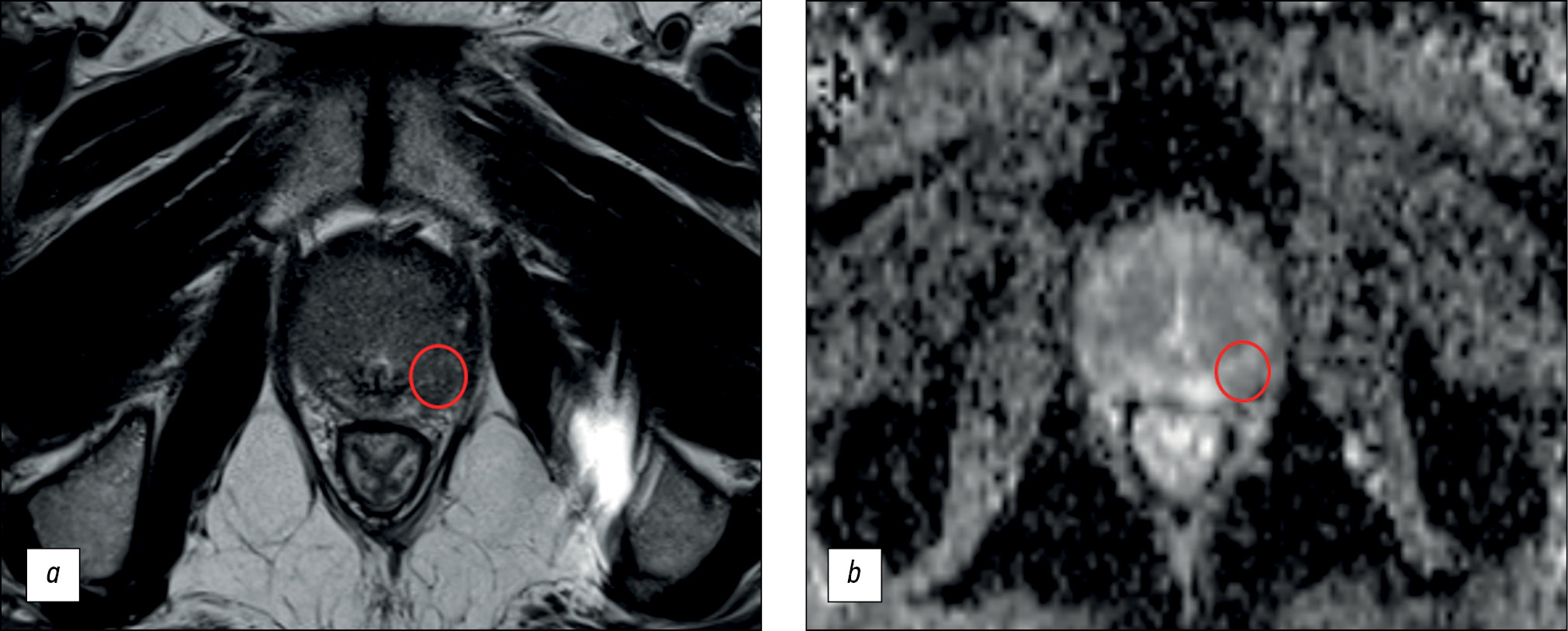
Рис. 1. Пример ложноположительного результата бипараметрической магнитно-резонансной томографии: а ― Т2-взвешенное изображение в аксиальной плоскости: в латеральном заднем сегменте периферической зоны левой доли в средней части предстательной железы отмечается очаг пониженного сигнала, соответствующий зоне ограничения диффузии; b ― карта измеряемого коэффициента диффузии. Данный очаг был охарактеризован врачом как PI-RADS5. По данным мультифокальной биопсии ― ткань предстательной железы без признаков опухолевого роста.
Второй вывод, который можно сделать из нашего исследования, свидетельствует, что выполнение мпМРТ ведёт к повышению диагностической эффективности метода за счёт роста показателей специфичности при интерпретации рентгенологами с опытом работы менее 2 лет (77,6 и 70,2% при бпМРТ) и более 5 лет (74,6 и 67,2% при бпМРТ).
Обсуждение основного результата исследования
Полученные результаты крайне близки к опубликованным в мировой научной литературе. Так, в работе J. Wallström и соавт. [6] применение мпМРТ позволило выявить один дополнительный случай опухоли (84 случая против 83). В ретроспективном исследовании под руководством C.K. Kuhl и соавт. [7] выполнение мпМРТ привело к обнаружению дополнительных 10 из 329 опухолей. В проспективном исследовании J.P. Zawaideh и соавт. [11] бпМРТ выявила 116 случаев рака, а мпМРТ ― 117. Не остались в стороне и метаанализы: так, в работах под руководством Z. Kang [12] и X.K. Niu [13] сообщалось о схожей диагностической точности бпМРТ и мпМРТ в отношении выявлении рака предстательной железы.
Наши данные противоречат результатам классического исследования PROMIS [14], согласно которому МРТ имела высокую чувствительность (93%), но, напротив, низкую специфичность (41%). Однако в указанной работе в качестве положительного результата МРТ учитывались, в том числе, и очаги PI-RADS 3. Отличались и гистологические критерии клинически значимого рака предстательной железы: не были включены очаги с оценкой 3+4 по шкале Gleason. Одной из причин неоптимальных показателей диагностической точности МРТ могло стать ненормальное распределение случаев нормы и патологии в нашей выборке.
Ключевым отличием мпМРТ является присутствие в протоколе сканирования ДКУ. В нашей работе показано, что за счёт применения ДКУ отмечается повышение специфичности выявления очагов предстательной железы у врачей с опытом менее 2 лет и более 5 лет (см. табл. 2 и 3; рис. 2); у врача-рентгенолога с опытом работы от 2 до 5 лет отмечалось парадоксальное снижение специфичности при оценке датасета мпМРТ.
Рис. 2. Пример повышения категории PI-RADS при использовании динамического контрастного усиления: а ― Т2-взвешенное изображение в аксиальной плоскости: в латеральном заднем сегменте периферической зоны правой доли в средней части предстательной железы отмечается очаг пониженного сигнала, соответствующий зоне ограничения диффузии; b ― карта измеряемого коэффициента диффузии: данный очаг был охарактеризован врачом как PI-RADS 3 при использовании биМРТ, однако при динамическом контрастном усилении (с) очаг демонстрирует раннее контрастное усиление, что позволяет расценить его как PI-RADS 4.
К недостаткам применения ДКУ в мпМРТ предстательной железы традиционно относят увеличение времени сбора данных, которое включает не только процесс введения контрастного вещества, но и подготовку к нему, включая катетеризацию пациента. Немаловажным моментом является увеличение времени анализа исследований с ДКУ, а также повышенные требования к программному обеспечению. Однако следует отметить некоторое увеличение диагностической точности с применением ДКУ (66,4 против 61,7% у рентгенолога с опытом работы менее 2 лет и 70,1 против 68,2% у рентгенолога с опытом работы более 5 лет).
Ещё одним аргументом в пользу бпМРТ являются опасения по поводу долгосрочной безопасности контрастных средств на основе гадолиния. Так, показано, что небольшое количество гадолиния может сохраняться в мозге и других тканях. Несмотря на то, что не было доказано никаких негативных последствий использования современных макроциклических контрастных средств в клинической практике у пациентов с нормальной функцией почек, с точки зрения безопасности можно утверждать, что контрастные средства для МРТ должны использоваться только в случаях, когда они добавляют значительную диагностическую ценность [15], что и было показано в нашем исследовании.
Как уже отмечалось, целью ДКУ в мпМРТ является дифференциальная диагностика очагов PI-RADS 3 и 4, локализованных в периферической зоне предстательной железы. В соответствии с критериями Epstein, клинически незначимый рак имеет сумму баллов по Глисону ≤6, ограничен органом (стадия по TNM <T3), имеет объём <0,5 см3, что должно быть определено на анатомическом препарате [16]. Это же определение используется в PI-RADS v2.1 [1]. Смысл выявления клинически незначимых опухолей заключается в возможности их активного наблюдения.
В нашей работе, в отличие от упомянутых выше исследований [6, 7], отмечалось уменьшение числа ложноположительных случаев выявления опухолей предстательной железы с применением ДКУ. Как следствие, это приводило к увеличению положительного прогностического значения теста. Схожие результаты были получены в работе J.P. Zawaideh и соавт. [11].
Выполнение ДКУ не изменит подхода к планированию биопсии предстательной железы при условии выявления очага PI-RADS 3 или выше. Следует принимать этот факт во внимание с учётом того, что трансректальная биопсия является инвазивной процедурой, сопряжённой с риском инфекционных осложнений и требующей госпитализации [17].
Ограничения исследования
Тем не менее следует понимать, что наше исследование имеет серьёзные ограничения. В первую очередь, ретроспективный дизайн исследования предполагал отбор пациентов исключительно с выполненной мультифокальной биопсией. Следовательно, распределение нормы и патологии в нашей выборке не соответствовало нормальному. Во-вторых, последовательный просмотр датасетов бпМРТ и мпМРТ рентгенологами, несмотря на двухнедельный washout-период (период вымывания), не позволял исключить предвзятость. В-третьих, небольшое количество рентгенологов, принимавших участие в исследовании, не позволяет сделать однозначный вывод о согласованности их оценок.
Нельзя не обратить внимания на умеренные значения согласованности между экспертами с небольшим (менее 2 лет) и значительным (более 5 лет) опытом работы, при этом отмечается рост согласованности с использованием мпМРТ. Данные литературы в отношении этого вопроса разнятся: так, в работе E.D. Campli и соавт. [18] не выявлено значимого влияния опыта рентгенолога на диагностическое качество обоих протоколов, однако в статье M. Gatti и соавт. [19] показано, что рентгенологи с небольшим опытом оценивают бпМРТ с меньшей точностью.
ЗАКЛЮЧЕНИЕ
МРТ предстательной железы показала неоптимальные показатели диагностической эффективности независимо от применяемого протокола сканирования. Несмотря на то, что бипараметрические протоколы сканирования предстательной железы имеют безусловное экономическое преимущество перед мультипараметрическими за счёт отсутствия расходов на контрастное вещество и расходные материалы и значительного снижения времени загрузки МР-сканера, их использование может привести к снижению диагностической точности метода.
Выявленная тенденция к улучшению чувствительности и специфичности метода с увеличением опыта рентгенолога свидетельствует о важности обучения правилам интерпретации МРТ предстательной железы согласно PI-RADS.
Для подтверждения роли бпМРТ в ранней диагностике рака предстательной железы требуется проведение проспективного исследования.
ДОПОЛНИТЕЛЬНО
Источник финансирования. Данная статья подготовлена авторским коллективом в рамках научно-исследовательской работы «Научное обоснование методов лучевой диагностики опухолевых заболеваний с использованием радиомического анализа», (№ ЕГИСУ: № 123031500005-2) в соответствии с Приказом от 21.12.2022 г. № 1196 «Об утверждении государственных заданий, финансовое обеспечение которых осуществляется за счет средств бюджета города Москвы государственным бюджетным (автономным) учреждениям подведомственным Департаменту здравоохранения города Москвы, на 2023 год и плановый период 2024 и 2025 годов» Департамента здравоохранения города Москвы.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Вклад авторов. Авторы подтверждают соответствие своего авторства международным критериям ICMJE (все авторы внесли существенный вклад в разработку концепции, проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию перед публикацией). Наибольший вклад распределён следующим образом: Ю.А. Васильев, О.В. Омелянская, А.В. Владзимирский ― концепция исследования; П.Б. Гележе, Р.В. Решетников ― анализ данных, написание текста статьи; А.П. Гончар, И.А. Блохин, И.И. Абдуллин, И.Н. Киева ― анализ данных.
1 The R Project for Statistical Computing. Режим доступа: https://www.r-project.org/.
2 irr: Various Coefficients of Interrater Reliability and Agreement. Режим доступа: https://cran.r-project.org/web/packages/irr/index.html.
3 dplyr: A grammar of data manipulation. Режим доступа: https://github.com/tidyverse/dplyr.
Об авторах
Юрий Александрович Васильев
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: npcmr@zdrav.mos.ru
ORCID iD: 0000-0002-0208-5218
SPIN-код: 4458-5608
канд. мед. наук
Россия, МоскваОльга Васильевна Омелянская
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: o.omelyanskaya@npcmr.ru
ORCID iD: 0000-0002-0245-4431
SPIN-код: 8948-6152
Россия, Москва
Антон Вячеславович Владзимирский
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: npcmr@zdrav.mos.ru
ORCID iD: 0000-0002-2990-7736
SPIN-код: 3602-7120
д-р мед. наук, профессор
Россия, МоскваПавел Борисович Гележе
Научно-практический клинический центр диагностики и телемедицинских технологий; Акционерное общество «Европейский Медицинский Центр»
Автор, ответственный за переписку.
Email: gelezhe.pavel@gmail.com
ORCID iD: 0000-0003-1072-2202
SPIN-код: 4841-3234
Россия, Москва; Москва
Роман Владимирович Решетников
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: reshetnikov@fbb.msu.ru
ORCID iD: 0000-0002-9661-0254
SPIN-код: 8592-0558
Россия, Москва
Анна Павловна Гончар
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: a.gonchar@npcmr.ru
ORCID iD: 0000-0001-5161-6540
SPIN-код: 3513-9531
Россия, Москва
Иван Андреевич Блохин
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: i.blokhin@npcmr.ru
ORCID iD: 0000-0002-2681-9378
SPIN-код: 3306-1387
Россия, Москва
Искандер Ильфакович Абдуллин
Научно-практический клинический центр диагностики и телемедицинских технологий
Email: iabdullin@emcmos.ru
ORCID iD: 0000-0003-1138-0822
SPIN-код: 6560-5219
Россия, Москва
Ирина Николаевна Киева
Детская городская клиническая больница № 9 имени Г.Н. Сперанского
Email: kieva.irina@gmail.com
ORCID iD: 0000-0002-4060-5966
SPIN-код: 2279-9141
Россия, Москва
Список литературы
- Turkbey B., Rosenkrantz A.B., Haider M.A., et al. Prostate imaging reporting and data system version 2.1: 2019 Update of prostate imaging reporting and data system version 2 // Eur Urol. 2019. Vol. 76, N 3. P. 340–351. doi: 10.1016/j.eururo.2019.02.033
- Bjurlin M.A., Carroll P.R., Eggener S., et al. Update of the standard operating procedure on the use of multiparametric magnetic resonance imaging for the diagnosis, staging and management of prostate cancer // J Urol. 2020. Vol. 203, N 4. P. 706–712. doi: 10.1097/JU.0000000000000617
- Rouvière O., Puech P., Renard-Penna R., et al. Use of prostate systematic and targeted biopsy on the basis of multiparametric MRI in biopsy-naive patients (MRI-FIRST): A prospective, multicentre, paired diagnostic study // Lancet Oncology. 2019. Vol. 20, N 1. P. 100–109. doi: 10.1016/S1470-2045(18)30569-2
- Boesen L., Thomsen F.B., Nørgaard N., et al. A predictive model based on biparametric magnetic resonance imaging and clinical parameters for improved risk assessment and selection of biopsy-naïve men for prostate biopsies // Prostate Cancer Prostatic Dis. 2019. Vol. 22, N 4. P. 609–616. doi: 10.1038/s41391-019-0149-y
- Tamada T., Kido A., Yamamoto A., et al. Comparison of biparametric and multiparametric MRI for clinically significant prostate cancer detection with PI-RADS Version 2.1 // J Magnetic Resonance Imaging. 2021. Vol. 53, N 1. P. 283–291. doi: 10.1002/jmri.27283
- Wallström J., Geterud K., Kohestani K., et al. Bi- or multiparametric MRI in a sequential screening program for prostate cancer with PSA followed by MRI? Results from the Göteborg prostate cancer screening 2 trial // Eur Radiol. 2021. Vol. 31, N 11. P. 8692–8702. doi: 10.1007/s00330-021-07907-9
- Kuhl C.K., Bruhn R., Krämer N., et al. Abbreviated biparametric prostate MR imaging in men with elevated prostate-specific antigen // Radiology. 2017. Vol. 285, N 2. P. 493–505. doi: 10.1148/radiol.2017170129
- Абуладзе Л.Р., Семенов Д.С., Панина О.Ю., Васильев Ю.А. Оптимизированный протокол бипараметрической магнитно-резонансной томографии для диагностики рака предстательной железы // Digital Diagnostics. 2022. Т. 3, № 3. C. 166–177. doi: 10.17816/DD108484
- Schoots I.G., Barentsz J.O., Bittencourt L.K., et al. PI-RADS committee position on MRI without contrast medium in biopsy-naive men with suspected prostate cancer: Narrative review // Am J Roentgenol. 2021. Vol. 216, N 1. P. 3–19. doi: 10.2214/AJR.20.24268
- Gleason D.F. Classification of prostatic carcinomas // Cancer Chemother Rep. 1966. Vol. 50, N 3. P. 125–128.
- Zawaideh J.P., Sala E., Shaida N., et al. Diagnostic accuracy of biparametric versus multiparametric prostate MRI: Assessment of contrast benefit in clinical practice // Eur Radiol. 2020. Vol. 30, N 7. P. 4039–4049. doi: 10.1007/s00330-020-06782-0
- Kang Z., Min X., Weinreb J., et al. Abbreviated biparametric versus standard multiparametric MRI for diagnosis of prostate cancer: A systematic review and meta-analysis // Am J Roentgenol. 2019. Vol. 212, N 2. P. 357–365. doi: 10.2214/AJR.18.20103
- Niu X.K., Chen X.H., Chen Z.F., et al. Diagnostic performance of biparametric MRI for detection of prostate cancer: A systematic review and meta-analysis // Am J Roentgenol. 2018. Vol. 211, N 2. P. 369–378. doi: 10.2214/AJR.17.18946
- Ahmed H.U., El-Shater Bosaily A., Brown L.C., et al. Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer (PROMIS): A paired validating confirmatory study // Lancet. 2017. Vol. 389, N 10071. P. 815–822. doi: 10.1016/S0140-6736(16)32401-1
- McDonald R.J., Levine D., Weinreb J., et al. Gadolinium retention: A research roadmap from the 2018 NIH/ACR/RSNA workshop on gadolinium chelates // Radiology. 2018. Vol. 289, N 2. P. 517–534. doi: 10.1148/radiol.2018181151
- Ploussard G., Epstein J.I., Montironi R., et al. The contemporary concept of significant versus insignificant prostate cancer // Eur Urol. 2011. Vol. 60, N 2. P. 291–303. doi: 10.1016/j.eururo.2011.05.006
- Loeb S., Vellekoop A., Ahmed H.U., et al. Systematic review of complications of prostate biopsy // Eur Urol. 2013. Vol. 64, N 6. P. 876–892. doi: 10.1016/j.eururo.2013.05.049
- Campli E.D., Pizzi D.A., Seccia B., et al. Diagnostic accuracy of biparametric vs multiparametric MRI in clinically significant prostate cancer: Comparison between readers with different experience // Eur J Radiol. 2018. N 101. P. 17–23. doi: 10.1016/j.ejrad.2018.01.028
- Gatti M., Faletti R., Calleris G., et al. Prostate cancer detection with biparametric magnetic resonance imaging (bpMRI) by readers with different experience: Performance and comparison with multiparametric (mpMRI) // Abdominal Radiol (New York). 2019. Vol. 44, N 5. P. 1883–1893. doi: 10.1007/s00261-019-01934-3
Дополнительные файлы