Difficulties in myocarditis diagnosis: a case report
- Authors: Poteshkina N.G.1,2, Kovalevskaya E.A.1,2, Sinitsyn V.E.3, Mershina E.A.3, Filatova D.A.3, Selivanova G.B.1, Shashkina Y.R.2
-
Affiliations:
- The Russian National Research Medical University named after N.I. Pirogov
- Moscow City Hospital 52
- Lomonosov Moscow State University Medical Research and Educational Center
- Issue: Vol 4, No 4 (2023)
- Pages: 605-615
- Section: Case reports
- Submitted: 14.07.2023
- Accepted: 31.08.2023
- Published: 15.12.2023
- URL: https://jdigitaldiagnostics.com/DD/article/view/546163
- DOI: https://doi.org/10.17816/DD546163
- ID: 546163
Cite item
Abstract
Myocarditis is often difficult to diagnose. The diagnostic difficulties include nonspecific symptoms or a “vague” clinical picture, absence of pathognomonic signs during physical examination, and endomyocardial biopsy, which is the “gold standard” of diagnosis of myocarditis, being an invasive procedure that is performed under strict indications in certain patients. Nevertheless, as radiology is rapidly developing, clinicians are now able to noninvasively diagnose symptoms of inflammatory myocardial damage, including edema and myocardial fibrosis, using cardiac magnetic resonance imaging. This article presents the clinical case of a young patient with symptoms of acute coronary syndrome, who showed no evidence of coronary artery disease. Myocarditis was suspected because of increased activity of cardiospecific enzymes and high levels of inflammatory markers, pronounced electrocardiography changes with positive dynamics, and recent infection. Magnetic resonance imaging was used to confirm myocarditis diagnosis. Thus, this case study demonstrates the role of imaging techniques in the differential diagnosis of ischemic and inflammatory heart diseases.
Full Text
BACKGROUND
Acute myocarditis is defined as a sudden inflammatory injury to the heart muscles. Worldwide, approximately 4–14 cases per 100,000 are reported annually, and 1%–7% die from the disease [1]. Therefore, timely diagnosis is extremely important for clinicians to establish prognosis and treatment strategies.
Poorly defined symptoms at onset, lack of specific clinical signs of myocarditis, minimal changes on physical examination [2], and infrequent use of endomyocardial biopsy as the “gold standard for diagnosis” lead to the underdiagnosis of this disease in real-world practice [3].
However, criteria for diagnosing myocarditis, such as the presence of a previous infection confirmed by clinical and/or laboratory data and the clinical and diagnostic signs of recurrent heart muscle injury remain relevant [4].
Clinical signs:
- Chest pain
- Arrhythmias of unknown origin
- Signs and symptoms of heart failure
- Syncopal episodes and/or sudden death prevented (successfully resuscitated)
- Cardiogenic shock: absence of coronary artery (CA) injury and other cardiovascular diseases that could cause this condition
Diagnostic criteria:
- Laboratory criteria, with grade of recommendation (GoR) C and level of evidence (LoE) 5:
- Increased:
- Troponins T and I
- Lactate dehydrogenase
- Creatine kinase-MB (CK-MB)
- N-terminal pro-B-type natriuretic peptide (NT-proBNP)
- Serum cardiac autoantibodies
- Increased:
- Imaging criteria:
- Electrocardiography (ECG), GoR C, and LoE 4: blockades, arrhythmias, and ST-T changes
- Electrocardiography (ECG), GoR C, and LoE 4: functional and/or structural changes
- Gadolinium-enhanced magnetic resonance imaging (MRI) of the heart, GoR A, and LoE 2: myocardial edema and/or late contrast enhancement
- Morphological criteria, GoR C, and LoE 4: endomyocardial biopsy results
The prevalence of myocarditis is underestimated because of nonspecific symptoms of its onset and/or asymptomatic course. Therefore, every clinical case is interesting for the possibility of diagnosing this disease.
CASE REPORT
Patient M (33 years old) had no comorbidities or family history of cardiovascular disease. He was a non-smoker with a physically active lifestyle. He was admitted to the cardiac intensive care unit for suspected acute coronary syndrome with ST elevation. On admission, he complained of severe retrosternal pain that was “searing and burning.”
Case History
Two days before his hospitalization, the described pain appeared for the first time while resting at night. It lasted for more than an hour and then disappeared spontaneously.
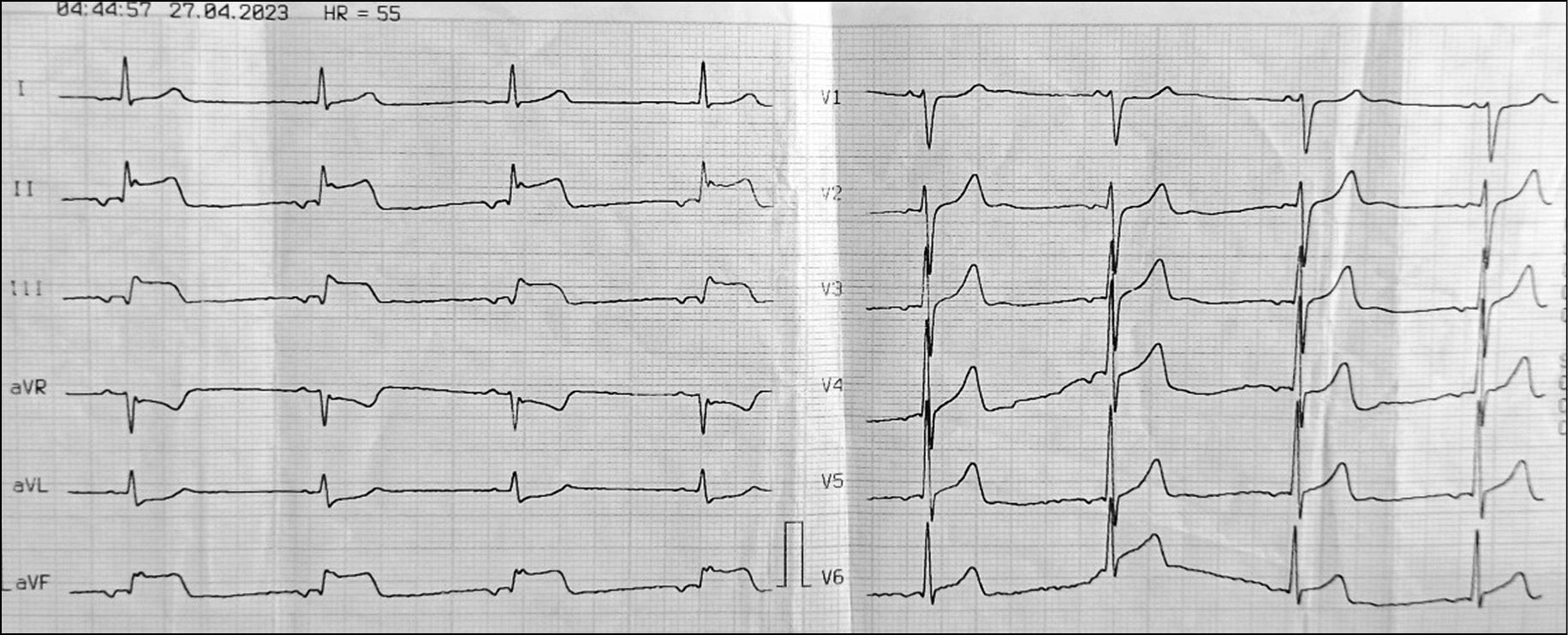
A similar pain attack recurred the next night. However, the pain syndrome lasted longer. ECG recorded by the emergency team showed an inferior atrial rhythm. The heart rate (HR) was 55 beats per minute. II, III, aVF, and V5–6 leads showed ST elevation up to 2 mm. aVR and aVL leads showed ST depression (Figure 1).
Fig. 1. Electrocardiography of patient M. at the prehospital stage.
The patient presented with severe retrosternal pain and ECG changes that were detected before hospitalization. The patient was treated with 10 mg of intravenous morphine, 600 mg of clopidogrel, and 250 mg of acetylsalicylic acid.
Examination
During admission, the patient’s consciousness was clear; the patient was cooperative, adequate, and oriented. The skin had normal color and moisture. His vital signs were as follows:
- Body temperature of 36.8℃
- Subcutaneous fat was moderately developed. The body mass index was 27.6 kg/m2. No peripheral edema
- Resting respiratory rate: 16 breaths/min
- Saturation: 98% in ambient air
- Blood pressure: 130/80 mmHg
- HR: 100 beats /min, the rhythm was normal
The left border of relative cardiac dullness in the fifth intercostal space was 1.5 cm medial to the left midclavicular line. The right border was along the right edge of the sternum. The upper border was in the third intercostal space.
Physiological accentuation of heart sounds was preserved. No heart murmurs were heard. Lung breathing was vesicular. No wheezing was heard. The abdomen was soft and painless. The liver was not enlarged (Kurlov ordinates were 10 × 8 × 7 cm). The spleen was not palpable. Stool and diuresis were normal.
C-reactive protein, antistreptolysin O, troponin I, and aspartate aminotransferase levels were elevated (Table 1).
Table 1. Laboratory data of patient M.
Parameter | Results | Reference |
Hemoglobin, g/L | 140 | 130–160 |
RBC, 10 12 /L | 5.04 | 4.00–5.00 |
WBC, 10 9 /L | 6.5 | 4.00–9.00 |
Lymphocytes, 10 9 /L | 2.5 | 2.0–6.5 |
C-reactive protein, mg/L | 10.45* | up to 6 |
Aspartate aminotransferase, U/L | 65* | up to 50 |
CK-MB, U/L | 1.0 | up to 25 |
Antistreptolysin O, GE/mL | 738.9* | up to 200 |
Total anticardiolipin antibodies, IU/L | 1.7 | up to 12 |
dsDNA IgG antibodies, IU/mL | 2.6 | up to 20.0 |
Antinuclear antibodies (semiquantitative) | 0.2 | up to 1.0 |
Troponin I (quantitative), ng/mL | 2.6* | up to 0.2 |
NT-proBNP | 54 | 0–125 |
Based on the clinical picture, ECG changes, and elevated cardiac enzymes on admission, the diagnosis was ST-elevation myocardial infarction. Emergency coronary angiography (CAG) was performed, which showed no stenotic lesions of the coronary bed in the left (Figure 2, a) and right (Fig. 2, b) coronary arteries. Signs of moderate peripheral vasospasm were observed (Figure 2).
Fig. 2. Coronary angiography of patient M.: a — left coronary artery; b — right coronary artery.
Based on ECHO-CG data, the left ventricular (LV) ejection fraction was 60%. No abnormalities in local contractility were reported. The diastolic function of the left ventricle was not affected. No signs of myocardial hypertrophy of the left ventricle were observed. The cardiac cavities were not dilated. The contractile function of the right ventricular (RV) myocardium was preserved. The systolic pressure of the pulmonary artery was 23 mmHg with grade 0–1 tricuspid regurgitation. Some pericardial thickening was detected.
Daily ECG monitoring showed the following:
- The main rhythm was sinus one with episodic sinus tachycardia, moderate sinus bradycardia, and sinus arrhythmia.
- The mean HR was 73 beats per minute.
- The maximum mean HR was 111 beats per minute.
- The minimum mean HR was 53 beats per minute.
- Three individual supraventricular extrasystoles occurred; no rhythm pauses lasting >2 s were reported.
- ST elevation was recorded up to 0.2–1.0 mm (in one lead).
Treatment
The patient was treated with angiotensin-converting enzyme inhibitors, mineralocorticoid receptor antagonists, and beta-blockers. During therapy, his condition improved, and the chest pain did not recur. Troponin I and inflammatory marker levels normalized within 10 days.
ECG showed positive changes (Figure 3):
- Focal myocardial changes in posterior phrenic and lateral LV walls in qR II, Qr III, and qr aVF leads.
- SR elevation in II, III, aVF, and V4–6 leads to 0.8 mm (over time, regression was >50% of the baseline one) with negative T waves in II, III, aVF, and V5–6 leads.
Fig. 3. ECG of patient M. in dynamics.
Clinical diagnosis
Therefore, according to ECHO-CG data, a young patient with severe chest pain had intact coronary arteries and preserved LVEF with no abnormalities in local/diffuse contractility. Moreover, the initial increase in troponin, antistreptolysin O, aspartate aminotransferase, and C-reactive protein levels was noted with significant positive ECG changes, so the diagnosis of myocarditis was discussed.
A detailed interview revealed that 10–12 days before admission, the patient had a sore throat and a fever exceeding 38℃ for 3 days. A nasopharyngeal swab was negative for coronavirus infection by polymerase chain reaction. The outpatient antibacterial therapy was reported to reduce fever and sore throat.
Since the infection was chronologically associated with clinical signs of the disease and pseudo-infarction ECG changes in the absence of coronary artery disease and with elevated cardiac enzymes, the possibility of acute myocarditis was high. To confirm the diagnosis, a cardiac MRI was performed using a gadolinium contrast agent.
The contrast-enhanced cardiac MRI did not show any enlargement of the heart chambers.
- An end-diastolic size (EDD) of the left ventricle was 52 mm.
- An indexed end-diastolic volume (EDV) of the left ventricle was 59 (reference, 59) mL/m2.
- The EDD of the right ventricle was 43 mm.
- The indexed EDV of the right ventricle was 72 (reference, 57–109) mL/m2).
- The sizes of the left and right atria were 41 and 48 mm, respectively.
The RV myocardium was 3–4 mm thick. No areas of local bulging or dyskinesia of the free RV wall were identified.
The LV myocardium was not hypertrophied: the thickness of the basal and middle segments did not exceed 10 mm, the thickness of the apical segments was 4–5 mm, and the indexed LV myocardial mass was 56 (reference, 41–86) g/ m2. Uniform thickening of the LV myocardium was reported during systole. No abnormalities in segmental contractility of the LV myocardium were detected. No decrease in overall LV contractility was reported with an LVEF of 64%.
No blood clots were found in the heart chambers. First-degree mitral regurgitation and first-degree tricuspid regurgitation were reported. The thoracic aorta had smooth contours and was not dilated, and the blood flow signal in its lumen was uniform. The pulmonary artery and its branches were not dilated. The superior and inferior vena cava were not dilated. In the pericardial cavity, trace amounts of free fluid were found at the level of the basal lateral LV and middle RV segments. The pericardial layers were not thickened, and the contrast agent did not accumulate. No hydrothorax was reported.
Signs of myocardial inflammation were noted including areas of early and delayed contrast enhancement in the basal and middle lateral and lower segments with the transition to the apical lower segment of the left ventricle (Figure 4a–c), as well as signs of myocardial edema in these segments (Figure 5a).
Fig. 4. Magnetic resonance imaging of the heart in delayed contrast mode with a gadolinium-containing contrast agent (7–15 minutes after administration of the contrast agent), pulse sequence Flash 2D Inversion Recovery: a, d — short axis of the left ventricle in the basal segments; b, e — long axis of the left ventricle, four-chamber view; c, f — long axis of the left ventricle, two-chamber view. Top row, a–c — magnetic resonance imaging of the heart initially: in the basal and middle lateral and inferior segments with a transition to the apical inferior segment of the left ventricle, subepicardial areas of contrast are noted (yellow arrows); bottom row, d–f — dynamic magnetic resonance imaging of the heart after 1.5 months: areas of delayed contrast of the previous localization and intensity remain.
Fig. 5. Magnetic resonance imaging of the heart in T2-mapping mode along the short axis of the left ventricle in the basal segments: a — magnetic resonance imaging of the heart initially: in the area of the lower and inferolateral segments there is an increase in the T2 relaxation time (>50 ms), which indicates presence of edema; b — magnetic resonance imaging of the heart in dynamics after 1.5 months: the native T2 parameter is within normal values (<50 ms). The numbers indicate the values of the T2 relaxation time in ms.
Conclusion on the cardiac MRI: MR signs of early subacute myocarditis (myocardial areas of early and delayed contrast enhancements in the lower and lateral LV walls with signs of edema).
Based on clinical, historical, laboratory, and instrumental data, the following diagnosis was made: acute infectious and allergic myocarditis, pseudocoronary clinical variant, subacute course; CAG: without stenotic lesions of the coronary arteries.
According to the Mayo Clinic, myocarditis classification [5] using baseline characteristics, the patient had a low risk of cardiovascular complications and a favorable prognosis (Table 2). However, an intermediate-risk group could be considered based on cardiac MRI data.
Table 2. Clinical variants of myocarditis onset (Mayo Clinic)
Low risk | Intermediate risk (“gray area”) | High risk |
Chest pain | Moderate persistent structural and functional changes in the myocardium | Severe persistent LV dysfunction and circulatory decompensation |
Supraventricular rhythm disorders | Nonsustained ventricular arrhythmias | Life-threatening arrhythmias |
AV block | No life-threatening rhythm and conduction disorders | Persistent AV block |
Preserved LVEF | Late gadolinium accumulation in the myocardium without cardiac chamber remodeling | Recurrent syncope |
Rapid response to therapy (1–4 weeks) | ||
Favorable prognosis | Uncertain prognosis | Unfavorable prognosis |
The patient was discharged with improvement. He was recommended to continue the prescribed therapy and subject to cardiac MRI over time.
After 1.5 months, the contrast-enhanced MRI of the heart showed that the area of subepicardial delayed enhancement of the previous extent remained in the basal and middle inferior segments (Figure 4d–f), and no evidence of myocardial edema was found in these segments (Figure 5b).
DISCUSSION
The guidelines of the European Society of Cardiology [6] and the Russian clinical guidelines for the diagnosis of myocarditis [4] emphasize the effectiveness of cardiac MRI. For this purpose, the Lake Louise criteria were developed and first published in 2009. They included the assessment of signal hyperintensity on T2-weighted images (T2WI), short T1 inversion recovery sequences, and delayed non-coronary enhancement [7].
As the effectiveness of the original Lake Louise criteria was limited by the subjective nature of the qualitative assessment of the above signs, the criteria were revised in 2018. They have been supplemented with parametric mapping, which allows the quantitative assessment of regional and global myocardial relaxation times T1 and T2 and extracellular volume (ECV). As a result, the new Lake Louise criteria have higher rates of sensitivity and specificity (88% and 96%, respectively) than the old Lake Louise criteria [8].
If at least one criterion in each category is met, cardiac inflammation is confirmed:
- T2WI signs of myocardial edema (myocardial T2WI hyperintensity or high T2 relaxation index) [9]
- T1WI signs of myocardial injury (non-ischemic pattern of delayed contrast enhancement or high T1 relaxation index and/or ECV) [10]
If only one marker is present, myocardial inflammation may be considered in the presence of clinical and/or laboratory manifestations; however, the specificity of MRI in this case is lower. Other signs of heart inflammation include systolic dysfunction (areas of hypokinesia or akinesia) and signs of pericarditis (contrast enhancement of the pericardial layers). The use of these criteria is warranted only when symptoms and signs of inflammatory heart diseases are present and not as a screening technique for asymptomatic patients [11, 12].
In this case report, contrast-enhanced cardiac MRI confirmed the clinical diagnosis. According to cardiac MRI, the patient initially had one of the above criteria for diagnosing myocarditis (myocardial edema on T2 mapping and evidence of non-ischemic myocardial injury on delayed gadolinium enhancement). MRI performed after 1.5 months showed no signs of myocardial edema, indicating a decrease in acute myocardial inflammation.
CONCLUSION
Therefore, contrast-enhanced cardiac MRI is a highly informative imaging modality for myocardial inflammation, for primary diagnosis and long-term assessment, allowing for definitive confirmation of the diagnosis.
ADDITIONAL INFORMATION
Funding source. This article was not supported by any external sources of funding.
Competing interests. The authors declare that they have no competing interests.
Authors’ contribution. All authors made a substantial contribution to the conception of the work, acquisition, analysis, interpretation of data for the work, drafting and revising the work, final approval of the version to be published and agree to be accountable for all aspects of the work. Poteshkina N.G. — development of the article concept, text writing; Kovalevskaya E.A. — text writing and reviewing, Sinitsyn V.E. — development of the article concept, approval of the final version of the text, Mershina E.A. — approval of the final version of the text, Filatova D.A. — text writing and reviewing, Selivanova G.B. — text writing and reviewing, Shashkina Y.R. — text writing and reviewing.
Consent for publication. Written consent was obtained from the patient for publication of relevant medical information and all of accompanying images within the manuscript in Digital Diagnostics Journal.
About the authors
Natalia G. Poteshkina
The Russian National Research Medical University named after N.I. Pirogov; Moscow City Hospital 52
Author for correspondence.
Email: nat-pa@yandex.ru
ORCID iD: 0000-0001-9803-2139
SPIN-code: 2863-4840
MD, Dr. Sci. (Med.), Professor
Russian Federation, Moscow; MoscowElena A. Kovalevskaya
The Russian National Research Medical University named after N.I. Pirogov; Moscow City Hospital 52
Email: tolyaaa@mail.ru
ORCID iD: 0000-0002-0787-4347
SPIN-code: 8853-2700
MD, Cand. Sci. (Med.), Assistant professor
Russian Federation, Moscow; MoscowValentin E. Sinitsyn
Lomonosov Moscow State University Medical Research and Educational Center
Email: vsini@mail.ru
ORCID iD: 0000-0002-5649-2193
SPIN-code: 8449-6590
MD, Dr. Sci. (Med.), Professor
Russian Federation, MoscowElena A. Mershina
Lomonosov Moscow State University Medical Research and Educational Center
Email: elena_mershina@mail.ru
ORCID iD: 0000-0002-1266-4926
SPIN-code: 6897-9641
MD, Cand. Sci. (Med.), Assistant professor
Russian Federation, MoscowDaria A. Filatova
Lomonosov Moscow State University Medical Research and Educational Center
Email: dariafilatova.msu@mail.ru
ORCID iD: 0000-0002-0894-1994
SPIN-code: 2665-5973
Russian Federation, Moscow
Galina B. Selivanova
The Russian National Research Medical University named after N.I. Pirogov
Email: galina.selivanova@rambler.ru
ORCID iD: 0000-0003-2980-9754
SPIN-code: 9711-5041
MD, Dr. Sci. (Med.), Professor
Russian Federation, MoscowYavilika R. Shashkina
Moscow City Hospital 52
Email: yavilika-medik@mail.ru
ORCID iD: 0000-0002-2194-0785
Russian Federation, Moscow
References
- Ammirati E, Moslehi JJ. Diagnosis and Treatment of Acute Myocarditis: A Review. JAMA. 2023;329(13):1098–1113. doi: 10.1001/jama.2023.3371
- Caforio ALP, Calabrese F, Angelini A, et al. A prospective study of biopsy-proven myocarditis: prognostic relevance of clinical and aetiopathogenetic features at diagnosis. European Heart Journal. 2007;28(11):1326–1333. doi: 10.1093/eurheartj/ehm076
- Leone O, Veinot JP, Angelini A, et al. 2011 Consensus statement on endomyocardial biopsy from the Association for European Cardiovascular Pathology and the Society for Cardiovascular Pathology. Cardiovascular Pathology. 2012:21(4):245–274. doi: 10.1016/j.carpath.2011.10.001
- Arutyunov GB, Paleev FN, Moiseeva OM, et al. 2020 Clinical practice guidelines for Myocarditis in adults. Russian Journal of Cardiology. 2021;26(11):4790. (In Russ) doi: 10.15829/1560-4071-2021-4790
- Schultz JC, Hilliard AA, Cooper LT, et al. Diagnosis and Treatment of Viral Myocarditis. Mayo Clinic Proceedings. 2009;84(11):1001–1009. doi: 10.1016/s0025-6196(11)60670-8
- Caforio ALP, Pankuweit S, Arbustini E, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. European Heart Journal. 2013;34(33):2636–2648. doi: 10.1093/eurheartj/eht210
- Friedrich MG, Sechtem U, Schulz-Menger J, et al. Cardiovascular Magnetic Resonance in Myocarditis: A JACC White Paper. Journal of the American College of Cardiology. 2009;53(17):1475–1487. doi: 10.1016/j.jacc.2009.02.007
- Tijmes FS, Thavendiranathan P, Udell JA, et al. Cardiac MRI Assessment of Nonischemic Myocardial Inflammation: State of the Art Review and Update on Myocarditis Associated with COVID-19 Vaccination. Radiology: Cardiothoracic Imaging. 2021;3(6):e210252. doi: 10.1148/ryct.210252
- Srichai MB, Lim RP, Lath N, et al. Diagnostic performance of dark-blood T2-weighted CMR for evaluation of acute myocardial injury. Investigative Radiology. 2013;48(1):24–31. doi: 10.1097/rli.0b013e3182718672
- Galán-Arriola C, Lobo M, Vílchez-Tschischke JP, et al. Serial Magnetic Resonance Imaging to Identify Early Stages of Anthracycline-Induced Cardiotoxicity. Journal of the American College of Cardiology. 2019;73(7):779–791. doi: 10.1016/j.jacc.2018.11.046
- Blagova OV, Pavlenko EV, Varionchik NV, et al. Myocarditis as a legitimate phenomenon in patients with primary noncompaction myocardium: diagnosis, treatment and impact on outcomes. Russian Journal of Cardiology. 2018;23(2):44–52. (In Russ) doi: 10.15829/1560-4071-2018-2-44-52
- Filatova DA, Mershina EA, Sinitsyn VE. COVID-19-related cardiac lesion: The questions of pathogenesis and diagnostics. Digital Diagnostics. 2023;4(2):156−169. (In Russ) doi: 10.17816/DD284706
Supplementary files