Diagnostic challenge: innovative approach in use of magnetic resonance imaging in aortic aneurysm
- Авторлар: Kobelev E.1, Pak N.T.1, Bobrikova E.E.1, Ussov W.Y.2, Kliver E.E.1, Sirota D.A.1, Chernyavskiy A.M.1, Bergen T.A.1
-
Мекемелер:
- E. Meshalkin National Medical Research Center
- Tomsk National Research Medical Center
- Шығарылым: Том 3, № 3 (2022)
- Беттер: 332-339
- Бөлім: Case reports
- ##submission.dateSubmitted##: 31.05.2022
- ##submission.dateAccepted##: 29.06.2022
- ##submission.datePublished##: 17.10.2022
- URL: https://jdigitaldiagnostics.com/DD/article/view/108404
- DOI: https://doi.org/10.17816/DD108404
- ID: 108404
Дәйексөз келтіру
Аннотация
Here we report a case of technological innovation: the use of magnetic resonance imaging to determine surgical strategy.
Here is a 47-year-old man who underwent an magnetic resonance imaging and subsequent surgical treatment of the aortic aneurysm. Unlike echocardiography, magnetic resonance imaging enabled us to view the entire thoracic aorta. Unlike computer tomography, magnetic resonance imaging enabled us to detect changes in the aortic wall accurately. Thus, in this case, the use of magnetic resonance imaging allowed us to determine the distal resection edge. The patient`s postoperative course was unremarkable. Use of electrocardiogram-synchronized magnetic resonance imaging of thoracic aorta allows detecting structural changes of the aortic wall and its mechanical properties. It is significant that magnetic resonance imaging results of the aortic wall correlate with histologic examination.
The extent of changes in the aortic wall must be determined to accurately plan surgical treatment of patients with aortic aneurism.
Magnetic resonance imaging of the aortic wall is promising for further study in multicenter research.
Негізгі сөздер
Толық мәтін
RELEVANCE
Patients with a thoracic aneurysm should be evaluated for prompt surgical intervention unless life expectancy from comorbid conditions is limited or quality of life is substantially impaired [1]. According to the most recent guidelines, the examination includes computed tomographic imaging or magnetic resonance imaging only for diameter measurements [2–4]. Here we report a new and unique MRI application to use in patients with a thoracic aneurism, which affects surgical strategy choice.
CASE REPORT
Here is a 47-year-old man who underwent an MRI and subsequent surgical treatment of an aortic aneurysm. The patient has no aggravating factors or chronic disease in the anamnesis.
Ascending aortic aneurysms is always a challenge for physicians. In the examination, echocardiography revealed dilatation of the ascending aorta up to 5.5 cm without aortic regurgitation.
The patient underwent an electrocardiogram (ECG)-synchronized MRI of the aorta and cardiac MRI. The study was performed on MRI 1.5T with a cardiac coil.
We used T2, T1 weighted scans without, and then with T1 weighted scan contrast enhancement. During MRI, was performed contrast enhancement angiography (Figure 1). The maximum diameter of the ascending aorta was 5.4 cm, the distance between proximal and caudal aneurismal edge was 9 cm. The diameter of the aorta before the orifice of the brachiocephalic trunk was up to 3.4 cm, between the orifices of the left common carotid and subclavian arteries — up to 2.4 cm, in the descending part — up to 2.3 cm. The distance from the edge of the brachiocephalic trunk to the cranial aneurismal edge was 5.5cm.
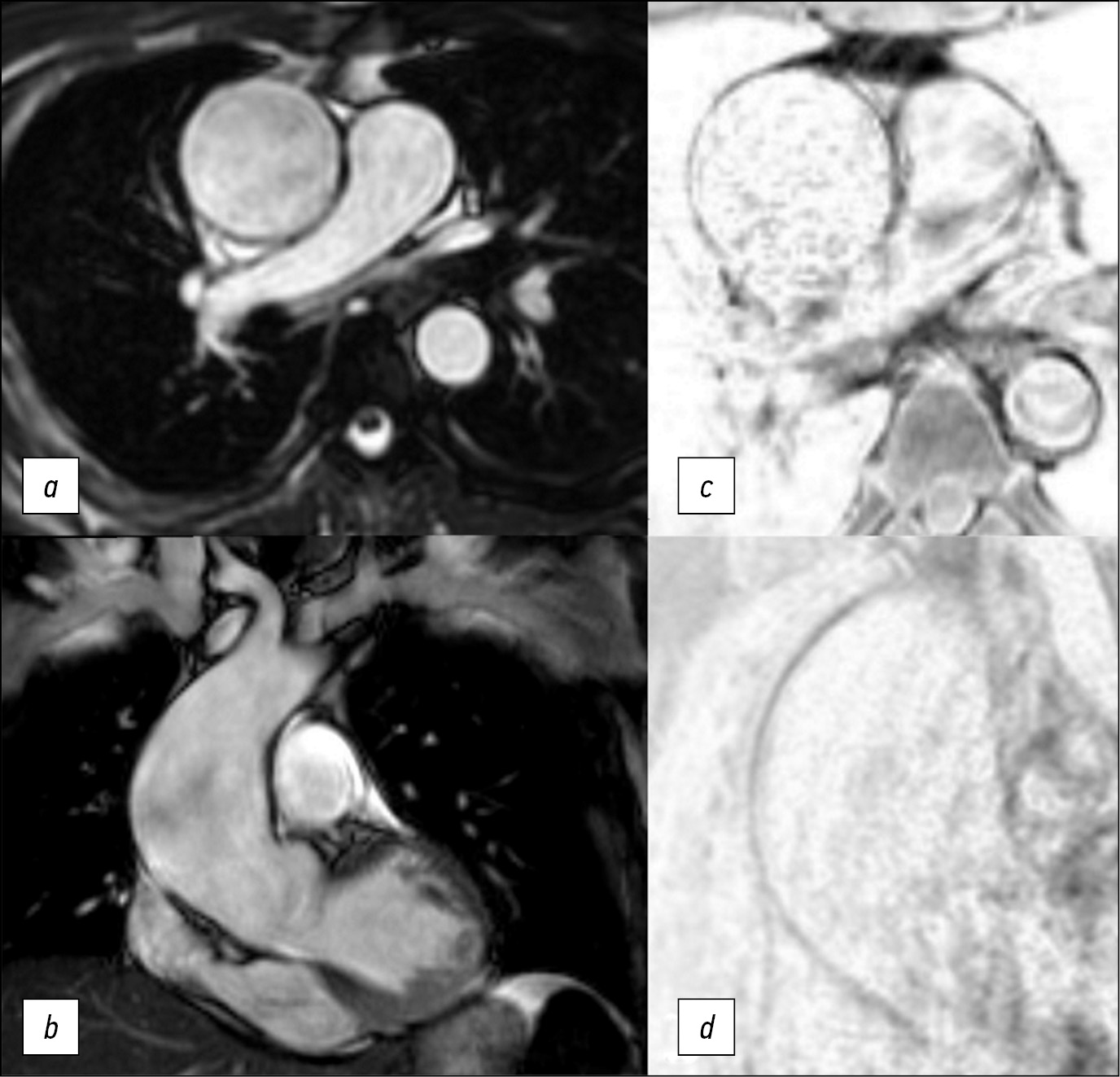
Fig. 1. Images obtained in the SSFP mode in the axial (a) and coronal (b) planes, T1-SE (middle third of the aortic aneurysm) in the axial plane (c), T1-SPIR in the "black blood" mode in the oblique plane (d ). Thinned wall of the aorta, more pronounced in the middle part.
As part of the study, sequences for aortic wall examination were performed.
To assess the aortic wall’s elasticity and contractility, we used native steady-state free-precession (SSFP) scans in the axial and coronary planes (Figure 1).
In the cine-SSFP view, we were able to clearly visualize the aortic wall’s movement during the cardio cycle and blood flow direction. The QFlow sequence can be used to quantify the pulse wave velocity in an aneurysm or if aortic valve function is required. To examine the ascending aorta wall’s thickness and vascularization, T1-spin-echo and gradient-echo in the axial plane, T1-spectrally selective suppression sequence and Spectral Presaturation with Inversion Recovery (SPIR) Black-Blood (BB) MRI (Fig. 2), T2-spectrally suppression sequence, and Black-Blood in the axial and oblique planes were performed.
Fig. 2. MR-contrast enhancement angiography, arterial phase, in breath-hold, in the oblique plane, 3D reconstruction of the aorta (a), T1-SPIR-BB imaging, axial plane (b) immediately after distal aneurysm edge of ascending aorta; oblique plane (c) before orifice of the brachiocephalic trunk. The intact thickness of the aortic wall (arrows), CT angiography of the thoracic aorta after surgical treatment (d).
According to the MRI conclusion, the patient has an enlarged ascending aorta from the root for up to 9 cm, with a maximum diameter of up to 5.5 cm. According to the modern guidelines a patient needs surgical treatment. The wall in the aneurysm is evenly thinned, more defined in the middle part, the pulsation is reduced, with signs of dyskinesia, from the edge of the aneurysm to the orifice of the brachiocephalic trunk – the aortic wall is intact (Figure 2) within no more than 3 cm, the aortic diameter at this level is no more than 3.5 cm. Additionally, the patient has a bicuspid aortic valve [1, 2, 4]. Dissection, thickening, and hypervascularization of the thoracic aorta wall and the proximal parts of its main branches were not revealed. The orifice of the main branches was typical anatomy.
DISCUSSION
Initially, during the existing strategy, it was planned to apply a clamp directly in front of the brachiocephalic trunk’s orifice, but, taking into account the MRI data, the surgical approach was adjusted. Considering the spread of the lesion of the aortic wall to the arcus distal to the aneurysm, it was decided to perform the intervention under conditions of circulatory arrest and antegrade unilateral cerebral perfusion. It is important that in case of resection and the pathology altered aortic wall, complications can be expected in the early and the late postoperative period. In this case, the patient underwent supracoronary prosthesis of the ascending part and the aortic arch with the formation of a distal anastomosis of the “half-arc” type.
After surgical treatment, a computer tomogram (CT) angiography of the thoracic aorta was performed (Figure 2). On postoperative scans, the diameter of the contrasting lumen of the aorta was not expanded. There were no endoleaks.
When comparing the MRI data with the histological examination results of intraoperative biopsy (resected aortic wall), the correspondence of the revealed changes in the aortic wall was noted. Macroscopically, the resected aorta’s wall thickness was found in distal and proximal edge 2.0-3.0 mm, in the middle part (including part of the distal aneurismal edge) 1.0-1.5 mm.
Microscopically, in sections from the proximal and distal parts of the aortic aneurysm and 2 cm from the distal resection edge: widespread destruction in the middle layer, mucoid swelling of elastic fibers, smoothing of the folds of elastic membranes were found. In some areas, closer to the adventitia, there are moderate scattered perivascular lymphoid infiltrations, part of the aortic wall’s vessels with obliteration of the lumens. Under the intima, there are focal accumulations of macrophages with foamy cytoplasm not protruding above the surface. (Fig. 3).
Fig. 3. Proximal (a, b) and middle (c) parts of the body of the aneurysm. Disseminated perivascular lymphoid infiltrate. Distal part of the resected aortic wall (d). All images show a picture of destruction, mucoid edema of elastic fibers, smoothing of elastic membrane folds.
Histopathological diagnosis: nonspecific secondary vasculitis of low activity, degradation of the aorta’s elastic membranes’ middle layer. Aneurysm of the ascending aorta. Atherosclerosis of the aorta, stage of lipid spots.
CONCLUSION
Unlike CT, MRI enables examining the structure and mechanical properties of an aortal wall and measurement of the diameter. In this case, an aortic wall MRI examination made it possible to choose the optimal surgical approach.
ADDITIONAL INFORMATION
Funding source. The work was carried out within the state assignment of the Ministry of Health of the Russian Federation (Development of tissue-engineered structures for cardiovascular surgery; N 121032300337-5).
Competing interests. The authors declare no conflict of interest.
Authors’ contribution. All authors made a substantial contribution to the conception of the work, acquisition, analysis, interpretation of data for the work, drafting and revising the work, final approval of the version to be published and agree to be accountable for all aspects of the work. T.A. Bergen, D.A. Sirota ― conception and design of the work; E. Kobelev, N.T. Pak, E.E. Kliver ― acquisition, analysis of data; E.E. Bobrikova, V.Yu. Usov ― interpretation of data; A.M. Chernyavskiy ― approved the final version of the work.
Consent for publication. Written consent was obtained from the patient for publication of relevant medical information and all of accompanying images within the manuscript in Digital Diagnostics journal.
Acknowledgments. We thank the Chief of the Institution of Experimental Biology and Medicine “E. Meshalkin National Medical Research Center” of the Ministry of Health of the Russian Federation MD Ph.D. professor Irina Yu. Zhuravleva for the opportunity to carry out this work.
Авторлар туралы
Evgenii Kobelev
E. Meshalkin National Medical Research Center
Email: kobelev_e@meshalkin.ru
ORCID iD: 0000-0002-5901-2271
SPIN-код: 7828-9713
Ресей, Novosibirsk
Natalya Pak
E. Meshalkin National Medical Research Center
Email: n_pak@meshalkin.ru
ORCID iD: 0000-0002-7842-9881
SPIN-код: 1896-8447
MD, Cand. Sci. (Med.)
Ресей, NovosibirskEvgeniya Bobrikova
E. Meshalkin National Medical Research Center
Email: bobrikova_e@meshalkin.ru
ORCID iD: 0000-0001-5985-4076
SPIN-код: 6315-9772
Ресей, Novosibirsk
Wladimir Ussov
Tomsk National Research Medical Center
Email: ussov1962@yandex.ru
ORCID iD: 0000-0001-7978-5514
SPIN-код: 1299-2074
MD, Dr. Sci. (Med.), Professor
Ресей, TomskEvgeniy Kliver
E. Meshalkin National Medical Research Center
Email: ee_kliver@meshalkin.ru
ORCID iD: 0000-0002-3915-3616
SPIN-код: 1511-3814
MD, Dr. Sci. (Med.)
Ресей, NovosibirskDmitriy Sirota
E. Meshalkin National Medical Research Center
Email: d_sirota@meshalkin.ru
ORCID iD: 0000-0002-9940-3541
SPIN-код: 4706-7549
MD, Cand. Sci. (Med.)
Ресей, NovosibirskAleksandr Chernyavskiy
E. Meshalkin National Medical Research Center
Email: a_cherniavsky@meshalkin.ru
ORCID iD: 0000-0001-9818-8678
SPIN-код: 5286-6950
MD, Dr. Sci. (Med.), Professor, Corresponding member of the Russian Academy of Sciences
Ресей, NovosibirskTatyanа Bergen
E. Meshalkin National Medical Research Center
Хат алмасуға жауапты Автор.
Email: bergen_t@meshalkin.ru
ORCID iD: 0000-0003-1530-1327
SPIN-код: 5467-7347
MD, Dr. Sci. (Med.)
Ресей, NovosibirskӘдебиет тізімі
- Erbel R, Aboyans V, Boileau C. et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The task force for the diagnosis and treatment of aortic diseases of the European society of cardiology (ESC). Eur Heart J. 2014;35(41):2873–926. doi: 10.1093/eurheartj/ehu281
- Hiratzka LF, Bakris GL, Beckman JA, et al. Guidelines for the diagnosis and management of patients with thoracic aortic disease. A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine. J Am Coll Cardiol. 2010;55(14):e27–e129.
- Galizia MS, Bolen MA, Flamm S. MRI of the thoracic aorta. Applied Radiology. 2015;44(8):22–26. doi: 10.37549/ar2207
- Saliba E, Sia Y. The ascending aortic aneurysm: When to intervene? IJC Heart Vasculature. 2015;6:91–100. doi: 10.1016/j.ijcha.2015.01.009
Қосымша файлдар