Left ventricular noncompaction with ventricular aneurysm in a 6-year-old patient
- Authors: Dautov T.B.1, Kaliyev B.B.1, Yerekesh B.T.2
-
Affiliations:
- «University Medical Center» Corporate Fund
- National Research Cardiac Surgery Center
- Issue: Vol 4, No 4 (2023)
- Pages: 625-632
- Section: Case reports
- Submitted: 17.07.2023
- Accepted: 06.09.2023
- Published: 15.12.2023
- URL: https://jdigitaldiagnostics.com/DD/article/view/551837
- DOI: https://doi.org/10.17816/DD551837
- ID: 551837
Cite item
Abstract
Ventricular noncompaction is a rare type of cardiomyopathy often associated with a ventricular aneurysm. We present a clinical case of a 6-year-old female who arrived at our clinic complaining of physical exertion. Echocardiography revealed prominent trabeculations in the left ventricular wall and a lateral-basal part bulging out, indicating noncompaction of the left ventricular myocardium with an aneurysm. With a noncompacted-to-compacted myocardium ratio of 2.6, magnetic resonance imaging revealed the presence of noncompacted myocardium. It also revealed impaired left ventricular systolic function and a left ventricular aneurysm with myocardial scarring. Coronary angiography ruled out coronary artery disease. Therefore, myocardial scarring was caused by noncompacted myocardium microcirculatory disorder.
Full Text
ABBREVIATIONS
Ao: aorta
CMR: cardiac magnetic resonance imaging
EF: ejection fraction
HF: heart failure
LA: left atrium
LGE: late gadolinium enhancement
LV: left ventricle
LVNC: left ventricular noncompaction
NC: noncompact myocardium
NC-to-C ratio: noncompact-to-compact ratio
RA: right atrium
RV: right ventricle
INTRODUCTION
Left ventricular noncompaction (LVNC) is a rare type of cardiomyopathy caused by myocardial compaction failure during embryogenesis. It has multiple prominent trabeculations with deep intertrabecular recesses [1]. Its clinical manifestations vary from no symptoms to cardiac dysfunction, heart failure (HF), arrhythmias, and systemic thromboembolism [2]. However, there are only a few reports of LVNC being aggravated by LV aneurysm [3], particularly in children, which is uncommon. Clinically, most LV aneurysms are asymptomatic, although they may cause arrhythmias (18.4%), embolic events (5.4%), rupture (4%), congestive HF (21.5%), and angina pectoris in rare cases [4]. In recent years, two major ideas on the development of LVNC have emerged: the embryogenesis hypothesis and the molecular genetic mechanism. Initially, it was believed that the inadequate consolidation of cardiomyocytes during abnormal embryonic morphogenesis led to the formation of prominent myocardial trabeculae and spaces between them. However, recent improvements in molecular genetic research techniques have revealed a growing number of genes associated with LVNC. Most identified genes are sarcomere protein genes, ion channel genes, and mitochondrial genes, with sarcomere protein genes most often implicated in pathogenesis [5]. In adults, the prevalence of isolated LVNC varies from 0.01% to 0.3% [6]. LVNC is classified as primary genetic cardiomyopathy by the American Heart Association. Conversely, the European Society of Cardiology classifies it under “unclassified cardiomyopathies” [7].
CASE REPORT
A 6-year-old female was admitted to our clinic with complaints of physical exertion. At 26 weeks of gestation, she had exudative pericarditis due to anamnesis. Echocardiography at 15 months revealed pericardial fluid up to 600 mL, prompting pericardiocentesis when the patient was diagnosed with hemopericarditis. Before admission, the patient was diagnosed with HF with a slightly decreased ejection fraction of LV (53). Body temperature was 36.6 C at the time of admission. SpO2 is 98%. The breath rate is 23 per minute. There is no organic noise in the heart tones, which are rhythmic and muffled. Blood pressure is 115/83 mmHg. The heart rate is 110 per minute.
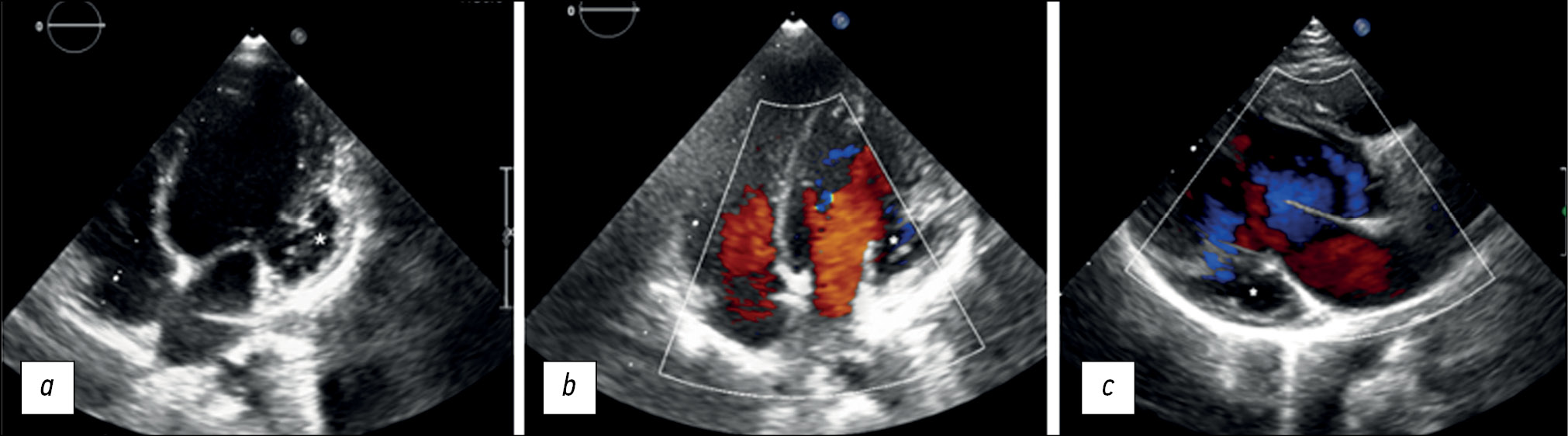
During hospitalization, echocardiography revealed LV dilatation, increased trabecularity of the apex and lateral wall of the LV, sac-like bulging of the lateral-basal part as aneurysm, and possibly deep trabeculae (Figure 1a–c). The echocardiography revealed a decline in LV systolic function and a 48% LV ejection fraction. There was minimal regurgitation on the tricuspid, mitral, and pulmonary valves.
Fig. 1. Transthoracic echocardiography (cardiac sensor, two-dimensional scanning) of a 6-year-old patient with myocardial non-compactness and left ventricular aneurysm: a - in the apical four-chamber projection in gray scale mode, bulging of the left ventricular wall and myocardial non-compaction are noted, the ventricle is connected to the aneurysm (asterisk); b — in the apical four-chamber projection in the color Doppler mapping mode, a large anechoic formation is determined (aneurysm is indicated by an asterisk) with pronounced trabeculation in the area of the apex and lateral walls of the left ventricle; c — in a three-chamber projection in the color Doppler mapping mode, the aneurysm (asterisk), inlet and outlet of the left ventricle are determined.
The main rhythm, according to the echocardiography, was sinus rhythm. The 24-h ECG Holter monitoring showed sinus rhythm, a mean heart ratio of −109 bpm, a minimum heart ratio of −64 bpm, a maximum heart ratio of −173 bpm, no pauses longer than 2 s, and no tachy-bradyarrhythmia.
A cardiac magnetic resonance imaging (CMR) with contrast enhancement (Gadobutrol 2.0 mL) was performed to exclude congenital heart diseases. The systolic function of both ventricles was reduced (LV EF [41%] and RV EF [45%]). The total LV mass of the myocardium was 54.6 g, with noncompacted myocardium accounting for 14.4 g or 26.3% of the total. CMR revealed signs of myocardial scarring and aneurysmatic ballooning of the basal anterior and lateral-basal walls of the left ventricle, noncompact myocardium (with an NC-to-C ratio = 2.6:1), and left ventricular dilatation. Accumulation of contrast media (one, five, and six segments) in delayed scans was observed (Figure 2a–e).
Fig. 2. Magnetic resonance imaging of the heart in a 6-year-old patient with myocardial non-compaction and left ventricular aneurysm. The scanning was carried out on a 1.5-T magnetic resonance imaging scanner (MAGNETOM Avanto, Siemens Healthcare, Germany) with breath holding: a - on a two-chamber image along the short axis before the introduction of a contrast agent, a well-defined protrusion of the lateral wall of the left ventricle (asterisk) and local thinning of the myocardium (arrows). Echo time (Time of echo) - 1.5 ms, repetition time (Repetition time) - 42 ms; b — on a four-chamber image along the long axis before the introduction of a contrast agent, an aneurysm (asterisk) in the basal part of the lateral wall of the left ventricle and non-compact myocardium are determined (the ratio of non-compact and compact layers is 2.6: 1). Echo time - 1.5 ms, repetition time - 42 ms; c - on a four-chamber long-axis image after contrast, there is late gadolinium enhancement (arrows) in the basal region of the anterolateral wall of the left ventricle, where the aneurysm is located (asterisk). Echo time - 1.5 ms, repetition time - 700 ms; d - on a two-chamber short-axis image after contrast, the accumulation of contrast agent in the first, fifth and sixth segments is determined. Echo time - 1.5 ms, repetition time - 2000 ms; e - Two-chamber long-axis image shows late gadolinium enhancement in the basal anterior wall of the left ventricle. Echo time is 1.4 ms, repetition time is 700 ms.
According to EchoCG and CMR, the patient has a noncompact left ventricular myocardium and aneurysm. Given the findings, it was decided to have a coronary angiography to assess the coronary vessels and exclude coronary artery anomalies. Coronary angiography showed no evidence of coronary artery abnormalities (Figure 4a and b).
Fig. 4. Coronary angiography of a 6-year-old patient with myocardial non-compaction and left ventricular aneurysm. The study was performed using a 4 Fr sheath and two 5 Fr catheters. a, b - no changes were detected in the coronary arteries; the left type of coronary blood supply is determined. RCA—right coronary artery; LAD—left anterior descending artery; Cx - circumflex artery; D1 - diagonal artery; RV branch - branch of the right coronary artery; AI is an intermediate branch.
Based on these findings, he was diagnosed with LVNC complicated by an aneurysm.
Given the examination results, weight gain, preserved tolerance to physical activity, and NT-proBNP level of 43.60 pg/mL, the patient was referred to a local hospital for continued monitoring with prescribed medication.
Treatment
Due to limited data on the treatment of this condition, it is recommended that clinical complications be managed in accordance with current guidelines for each specific complication. Anticoagulation therapy is recommended in LVNC patients with a history of thromboembolism, atrial fibrillation, and/or impaired systolic function (LV ejection fraction of <40%) due to an increased risk of thrombus formation resulting from deep intertrabecular recesses and slow blood flow [6]. Therefore, it is suggested that anticoagulation therapy may be necessary in patients with LVNC and accompanying LV aneurysms, even in the absence of systolic dysfunction or atrial fibrillation. However, there have been reports of patients undergoing more radical therapy, including surgical removal, to prevent stress and rupture of the aneurysm wall and the risk of thrombus formation. Furthermore, excising the fibrotic tissue of the LV aneurysm could help prevent arrhythmias, and reshaping the ventricle could improve the patient’s HF symptoms. Surgery is considered a definitive treatment that can be used in conjunction with optimal medical therapy [8].
DISCUSSION
The diagnosis of LVNC is mainly based on imaging anatomical characteristics. Although there is no universally established definition of LVNC, the following echocardiographic criteria are widely accepted: (a) two-layered myocardium with multiple, prominent trabeculations in end-systole; (b) NC-to-C ratio of >2; (c) Doppler color flow within the recesses and communication between the intertrabecular space and LV; and (d) absence of coexisting cardiac abnormalities. The classic triad of complications comprises HF, ventricular arrhythmia, and systemic embolic events [9].
We encountered a rare case of LVNC with an LV aneurysm formation due to microcirculatory disorder. As demonstrated in our patient, the CMR criterion for diagnosing LVNC is a ratio of maximum thickness between the noncompaction and compaction layer of more than 2.3 in end-diastole, and the mass of trabeculated lv myocardium represents >25% of the total LV mass [10]. Myocardial delayed enhancement revealed scars along the aneurysm wall. Aneurysms have a large connection to the ventricular cavity (Figure 3), whereas diverticula are typically elongated and have a narrowed neck. Aneurysms are most commonly observed in the LV apex (28%) and the perivalvular area close to the mitral valve (49%). LV aneurysms are typically acquired following an acute myocardial infarction with systolic bulging and scar formation in the myocardium. Without knowledge of the patient’s medical history and coronary angiogram, acquired aneurysms are difficult to distinguish from congenital left ventricular aneurysms [11]. However, poor microcirculation is believed to be the etiology of aneurysm and scar formation in LVNC [12]. The aneurysm was unrelated to coronary artery territory because our patient’s coronary angiography was normal. In our case, an aneurysm appears to be acquired because her previous echocardiography analysis showed EF above 50%; subsequently, when symptoms of cardiac failure began to manifest, it began to diminish. Complications from ventricular aneurysms include intramural thrombus, cardiac output impairment, and aneurysm rupture.
Fig. 3. Non-compactness of the myocardium with a thin-walled aneurysm of the left ventricle. The aneurysm bulges from the basal portion of the anterior wall of the left ventricle during systole. Arrows show the direction of blood flow. Ao - aorta; LA - left atrium; LV - left ventricle; NCM—non-compact left ventricular myocardium; RA - right atrium; RV - right ventricle; aneurism - aneurysm.
TEACHING POINT
A highly uncommon variant of cardiomyopathy is the combination of ventricular noncompaction and ventricular aneurysm. Echocardiography, CMR, and coronary angiography are valuable techniques for identifying the components of LVNC. Surgery can be combined with medical treatment, regardless of the prevalence of symptoms.
ADDITIONAL INFORMATION
Funding source. This article was not supported by any external sources of funding.
Competing interests. The authors declare that they have no competing interests.
Authors’ contribution. All authors made a substantial contribution to the conception of the work, acquisition, analysis, interpretation of data for the work, drafting and revising the work, final approval of the version to be published and agree to be accountable for all aspects of the work. Dautov TB ― contribution to the study concept, approved the final version of the work; Kaliyev BB ― revising and editing the manuscript; Yerekesh BT ― data sources collection and analysis, preparation of the manuscript.
Consent for publication. Written consent was obtained from the patient’s legal represantatives for publication of relevant medical information and all of accompanying images within the manuscript.
About the authors
Tairkhan B. Dautov
«University Medical Center» Corporate Fund
Email: tairkhan.dautov@mail.ru
ORCID iD: 0000-0002-5267-0108
SPIN-code: 8632-6605
MD, Dr. Sci. (Med.), Assistant Professor
Kazakhstan, AstanaBauyrzhan B. Kaliyev
«University Medical Center» Corporate Fund
Author for correspondence.
Email: baur233113@mail.ru
ORCID iD: 0000-0003-4825-749X
SPIN-code: 7315-9129
Kazakhstan, Astana
Bibissara T. Yerekesh
National Research Cardiac Surgery Center
Email: bibisara_97@mail.ru
ORCID iD: 0009-0002-0185-3278
Kazakhstan, Astana
References
- Srivastava S, Yavari M, Al-Abcha A, Banga S, Abela G. Ventricular non-compaction review. Heart Failure Reviews. 2022;27(4):1063–1076. doi: 10.1007/s10741-021-10128-3
- Petersen SE, Jensen B, Aung N, et al. Excessive Trabeculation of the Left Ventricle. JACC: Cardiovascular Imaging Expert Panel Paper. 2023;16(3):408–425. doi: 10.1016/j.jcmg.2022.12.026
- Catalano MA, Hemli JM, Lasic Z, Patel NC. Repair of left ventricular aneurysm in the setting of noncompaction. Journal of Cardiology Cases. 2022;25(6):416–419. doi: 10.1016/j.jccase.2022.01.008
- Tilahun T, Kedir E, Eshetu B. Fatal Left Ventricular Aneurysm in a 13 Years Old Male Child: A Case Report. Ethiopian journal of health sciences. 2021;31(4):903–906. doi: 10.4314/ejhs.v31i4.26
- Tian S, Liang H, Li X, et al. A novel mutation in the TTN gene resulted in left ventricular noncompaction: a case report and literature review. BMC Cardiovascular Disorders. 2023;23(1):352. doi: 10.1186/s12872-023-03382-w
- Yakabe D, Matsushima S, Uchino S, et al. Left Ventricular Noncompaction with Multiple Thrombi in Apical Aneurysm. Internal Medicine. 2020;59(3):377–381. doi: 10.2169/internalmedicine.3489-19
- Gerecke BJ, Engberding R. Noncompaction Cardiomyopathy-History and Current Knowledge for Clinical Practice. Journal of Clinical Medicine. 2021;10(11):2457. doi: 10.3390/jcm10112457
- Daprati A, Sassi CG, Garatti A, Saitto G, Menicanti L. Congenital left ventricular aneurysm with myocardial noncompaction pattern. Asian Cardiovascular and Thoracic Annals. 2020;28(8):504–506. doi: 10.1177/0218492320949833
- Ogah OS, Iyawe EP, Orimolade OA, et al. Left ventricular noncompaction in Ibadan, Nigeria. The Egyptian Heart Journal. 2023;75(1):69. doi: 10.1186/s43044-023-00396-9
- Gaižauskienė K, Glembockytė G, Glaveckaite S, Valevičienė N. Magnetic resonance diagnostic criteria of non-compaction cardiomyopathy: new diagnostic criteria still needed? Seminars in Cardiovascular Medicine. 2023;29(1):1–13. doi: 10.2478/semcard-2022-0003
- Ohlow MA. Congenital left ventricular aneurysms and diverticula: an entity in search of an identity. Journal of Geriatric Cardiology. 2017;14(12):750–762. doi: 10.11909/j.issn.1671-5411.2017.12.005
- Siripornpitak S, Khositseth A, Sriprachyakul A. Left Ventricular Non-compaction with Ventricular Aneurysms. Journal of Cardiovascular Imaging. 2020;28(3):222–225. doi: 10.4250/jcvi.2019.0091
Supplementary files